Bileşik Nedir, Bileşik Özellikleri Nelerdir?

İki ya da daha fazla elementin, kimyasal bir tepkime ile birlikte oluşturdukları saf maddeler, Kimya dünyasında bileşik olarak tanımlanıyor. Bileşik nedir, bileşik özellikleri ve çeşitleri nelerdir? Sorularına yanıt vermek adına buradayız ve dilerseniz daha fazla vakit kaybetmeden başlayalım. Bileşikleri detaylı bir şekilde incelediğimizde ihtiyacımız olacak çok özel bir detay karşımıza çıkıyor ve en küçük yapı taşının moleküller olduğunu da net bir şekilde görebiliyoruz.
Bileşik Nedir?
Bileşik hakkında araştırma yaptığınızda birçok kaynakta aynı bilgilerin yer aldığını göreceksiniz çünkü bu tanımlama ve özellikler değişmeyen, yani sabit özelliklerdir. 1799 yılında Proust tarafından keşfedilmiş ve devamında geliştirilmiştir. Bir element ya da bileşik, saf madde olarak nitelendirilir ancak bunların dışındaki maddelere baktığımızda karışım olarak nitelendirildiğini görebiliyoruz.
Ek bir bilgi daha verelim ve bu bilgiye de ihtiyacınızın olacağını düşünüyoruz. Element, aynı cins atomlardan meydana gelir. İki ya da çok daha fazla atomun bir araya gelmesi ise karşımıza molekülleri çıkartıyor. Bileşikler ile devam ediyoruz ve bu maddelerin baz, oksit ve tuz olarak sınıflandırıldığını da belirtmekte fayda var. İçerdikleri element türlerine göre isimlendirme yapmak da mümkündür ve bu sınıflandırma da metal ametal bileşikleri, metal kök bileşikleri ve ametal ametal şeklinde karşımıza çıkıyor.
Dilerseniz bileşikleri daha detaylı bir biçimde incelemek adına bir alt başlığa geçiş yapalım ve iki farklı sınıfta ele alalım.
Anorganik Bileşikler: İçeriğine göz attığımızda iyonlardan oluştuğunu gördüğümüz yapılanmalardır. Tuzlar ile birlikte bazları da bu sınıfa dahil edebiliyoruz. Bu sınıftaki bileşiklerin en büyük özelliği ise kararlı bileşikler olmalarıdır ve çabuk bozunmadıklarını da hatırlatmak gerekiyor.
Organik Bileşikler: Karbon bileşikleri olarak adlandırmak da mümkündür ve zaten birçok kaynakta da bu isim ile karşımıza çıkıyorlar. Kararsız bileşikler olduklarını da hatırlatmak gerekiyor ve onları bir arada tutan en güçlü kuvvet de elektron bağları olarak biliniyor.
Kimyasal bileşiklere geçiş yaptığımızda ise yine iki farklı sınıf karşımıza çıkıyor. Bileşik nedir, bileşik özellikleri ve çeşitleri nelerdir? Sorusuna yanıt vermeye devam ediyoruz.
Moleküler Bileşik: Moleküllerden meydana geldiklerini söyleyebiliriz. Kimyasal formüller ile ifade edilirler ve bu şekilde anılırlar.
İyonik Bileşik: Negatif ve pozitif iyonların bir çekim ile birleşimi sonucu ortaya çıkan yapılardır. Gerçekleşen alış veriş neticesinde elektron verenler katyon, alanlar ise anyon olarak biliniyor.
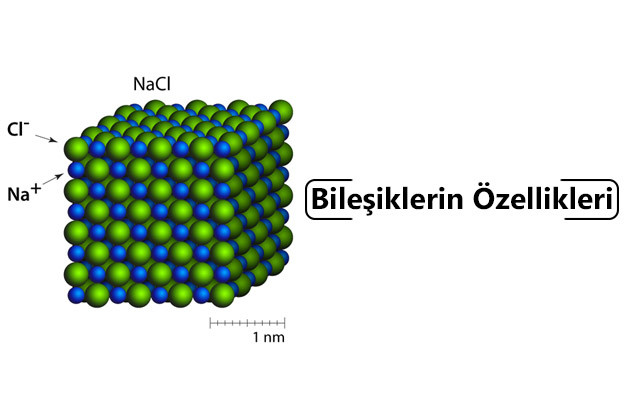
Bileşiklerin Özellikleri
Bileşik nedir, bileşik özellikleri ve çeşitleri nelerdir? Araştırması sonucunda bu konuyu aydınlatmaya devam ediyoruz. Dilerseniz şimdi de özellikler konusunu ele alalım ve sorularınıza da daha detaylı bir şekilde yanıt vermeye çalışalım.
- Bileşiklerin büyük bir kısmı moleküler yapıdadır ve bu şekilde karşımıza çıkıyorlar.
- Bileşik olabilmeleri için en az iki farklı cins elementin bir araya gelmesi gerekiyor. Aksi takdirde bileşik olarak nitelendirmek mümkün olmayacaktır.
- Kendisini oluşturan atomlar ile herhangi bir benzerlik göstermez ve tamamen farklı yapıya sahiptir.
- En önemli özellikleri ise saf madde olmalarıdır.
- Kimyasal yöntemler kullanılarak daha basit maddelere dönüştürülmeleri ise mümkündür ve oldukça kolaydır.
- 4 milyondan fazla bileşikten bahsediliyor ve elbette her biri ayrı ayrı tespit edilebilmiş değildir.
- Kovalent bağ ya da iyonik yapıdan meydana geldiklerini de bilmeniz gerekiyor.
- Bileşikler, birbirleri ile tepkimeye girebiliyor ve yine farklı bileşikleri oluşturabiliyorlar.
- Bileşik oluşumu ile birlikte parçalanma işleminde de enerji açığa çıkacaktır.
- Fiziksel yollarla bileşenlerine ayrılmaları mümkün değildir ve bu işlemin kimyasal yollarla yerine getirilmesi gerekir.
- Asit, baz, tuz ve oksitler şeklinde sınıflandırmak mümkündür.